Plate-forme « Cours en ligne » de l'université Blida1
Résultats de la recherche: 1398
A natural product is defined as a chemical compound or substance derived from living organisms found in nature. In its broadest sense, the term encompasses all substances produced by life in its various forms. Natural products are not limited to those extracted directly from biological sources but also include compounds synthesized in laboratories through chemical synthesis (both complete and partial). These compounds have played a pivotal role in the development of organic chemistry, serving as complex synthetic targets that have spurred innovation in the field. Furthermore, the commercial scope of the term has expanded to include cosmetics, dietary supplements, and foods derived from natural sources without artificial additives.
- Enseignant: Boukaabache Rabiaa

The aim of chemistry is to increase our understanding of the composition,
properties and change of matter. Claims and explanations in chemistry should be supported
by observational data.
The objectives of chemistry practical is :
(1) Enhancing students' understanding of scientific methodology. '
(2) A chance for students to learn science in a more tactile, engaging way.
(3) Complementing underlying scientific theory.
(4) Developing technical skills.
(5) Imparting scientific methodology.
(6) Enhancing transferable/soft skills (communication, time management, etc.).
- Enseignant: Aggoun amele
- Enseignant: Chetouane S.
- Enseignant: Chetouane Samia
Pour obtenir le code d'accès veuillez me contacter: samialaradj@yahoo.fr
Matière : Chimie des eaux
Crédits : 5
Coefficient : 3
A l'issue de ce module, l'étudiant sera capable:
- D'expliquer les anomalies des propriétés physiques et chimiques de l'eau et de leurs conséquences.
- De modéliser et comprendre les interactions solvant-solvant et solvant-soluté dans l'eau.
- De prévoir la réactivité de substances chimiques organiques ou minérales et le comportement de polluants.
contenu de la matière:
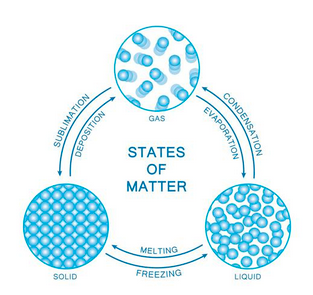
Chapitre 1 : propriétés physico-chimiques de l'eau
Différents états de l'eau- Diagramme d'état de l'eau pure.
Chapitre 2 : Cinétique chimique
Vitesse de la réaction
Réactions complexes
Influence de la température sur la vitesse de la réaction
La catalyse
Chapitre 3 : Propriétés des fonctions organiques
Effet électroniques dans les molécules organiques
Notions de réactifs chimiques et d'intermédiaires réactionnels
Composés halogénés
Alcools et phénols
Les amines
Les Aldehydes et Cétones
- Enseignant: ELMAHDI Ibtissem
Matériaux organiques et inorganiques

- Dr.: FS S2 Découverte
- Dr.: Ouradi Adel
Ce cours vise à étudier: la constitution du système olfactif et
par conséquent comprendre son fonctionnement;. Ensuite avoir un aperçu sur la nature chimique des molécules odorantes, les
voies de leur obtention et leur analyse; Enfin trouver et comprendre la
relation entre la structure et l’odeur de la molécule.
- Enseignant: bouzidi naima
Les produits naturels sont des molécules que l’on obtient de la nature (origine animale, végétale ou microorganismes).
Les plantes représentent une source immense de molécules chimiques complexes exploitées par l’homme dans l’industrie des parfums, agro-alimentaire, cosmétique et pharmaceutique.
Ce cours renferme l’étude de l'état naturel, des méthodes d'extraction, des propriétés physicochimiques, des méthodes de synthèses et hémisynthèse de:
1- Les terpènes;
2- les stéroïdes,
3- les saponosides
4- les alcaloïdes,
5- les composés phénoliques.
- Enseignant: Touafek Ouassila
La chimie fait partie des disciplines essentielles que doit maîtriser tout étudiant suivant un parcours de formation dans le domaine des Sciences de la Nature et de la Vie (SNV). Ce support pédagogique, confectionné selon le programme officiel du socle commun SNV, présente sous une forme simplifiée les notions fondamentales de la chimie des solutions et de la thermodynamique. En effet, plusieurs chapitres sont réservés pour un rappel de l’essentiel des notions théoriques avec de nombreuses applications pour clarifier et faciliter l’assimilation des points abordés.
A la fin de chaque chapitre des exercices et leurs solutions sont présentés permettront à l’étudiant d’appliquer les connaissances acquises et d’évaluer son niveau.
L'objectif principal de cet enseignement est de permettre aux étudiants, suivants des formations dans le domaine SNV, l'acquisition des connaissances de base en chimie requises en spécialité (analyses, biochimie)
Smain MEGATELI est maître de conférences classe A à la faculté des sciences de la nature et de la vie de l’université Saad Dahlab- Blida 1 où il enseigne la chimie et ses applications dans le domaine de l’agroalimentaire.
Objectif du Cours :
- Comprendre les principes fondamentaux de la chimie expérimentale.
- Acquérir des compétences pratiques en manipulation d'instruments et en techniques de laboratoire.
- Appliquer les concepts théoriques à des expériences concrètes.
Public Cible :
- Étudiants M1 (chimie Appliquée).
Prérequis
:
une connaissance de base en chimie expérimentale.
les montages utilisée en synthèse
Durée :
3H par semaine pendant un semestre
Contenu
du Cours :
Évaluation :
Contrôle continue, comptes rendus, examen écrit
- Enseignant: hamza kahina
Le cours de CHIMIE GENERALE est destiné pour les étudiants de 1ere année de l'institut des sciences et technique appliquées de l'université de Blida 1.

La chimie organique est la chimie des composés du carbone.
Mr LEFKIR Nadir

Ce cours est une introduction à la Chimie organique pharmaceutique. Il fait appel à plusieurs domaines frontières entre divers champs disciplinaires (chimie Organique, Chimie Pharmaceutique, et biomolécules). Cette discipline s'intéresse à la conception, à la préparation et à l'interprétation du mode d'action des médicaments, et plus spécifiquement, ceux issus de la synthèse organique. C'est une science qui tente, entre autres, d'établir des relations entre la structure chimique des drogues et leur activité biologique. Ce cours a donc pour vocation de familiariser l'étudiant avec les principes actifs des médicaments, leurs structures chimiques, leur origine, leur conception, leur évolution, leur domaine d'utilisation.
Public cible: Ce cours de CHimie organique pharmaceutique est destiné aux étudiants du 3ème année licence spécialité chimie pharmaceutique.
Objectifs:
Le but de cette formation est de maîtriser les concepts, les principes et les méthodes de la chimie organique, dont les objets d'investigation sont d'une grande importance sur le plan théorique et pratique. Au terme du cours, les étudiants doivent être capables de faire le lien entre une formule de structure et l'interaction du médicament avec le vivant. Ils doivent pouvoir tenir un discours critique sur les corrélations structure-pharmacodynamique ("drug design", pharmacophore, actions diverses possibles d'une molécule sur un récepteur donné) et les corrélations structure-pharmacocinétique (passage des barrières physiologiques, pKa, logP, stabilité chimique et photochimique).
- Enseignant: Aissaoui Meriem
Ce cours est une introduction à la Chimie organique pharmaceutique. C'est une science qui tente, entre autres, d'établir des relations entre la structure chimique des drogues et leur activité biologique. Ce cours a donc pour vocation de familiariser l'étudiant avec les principes actifs des médicaments, leurs structures chimiques, leur origine, leur conception, leur évolution, leur domaine d'utilisation.
Ce cours de Chimie organique pharmaceutique est destiné aux étudiants du 3ème année licence spécialité chimie pharmaceutique.
- Enseignant: ESSEID chahrazed

Description générale : La matière chimie physique appliquée étudie les mécanismes et les comportements rhéologiques des fluides complexes .
Objectifs généraux : La matière vise à :
-reconnaître la physico-chimique des systèmes biologiques ,
-Expliquer les interactions et la structure des produits complexes tels que les émulsions et leurs rôles dans l'approche moderne de la formulation .
Public cible : Ce cours est dédié aux étudiant de 3 ème Année Licence Technologie de Céréales .Département Agroalimentaire -Faculté SNV . Université de blida1;
- Enseignant: REBZANI FERAYALE
Ce cours permettra aux étudiants de Master 1 d'appliquer les méthodes de calcul théorique à la recherches des propriétés moléculaires à l'aide des logiciels de modélisation moléculaire.
- Enseignant: Ati Fella

La chimie verte est une branche de la chimie qui vise à concevoir des produits chimiques et des procédés de production qui réduisent ou éliminent l'utilisation et la génération de substances dangereuses. Son objectif principal est de promouvoir la durabilité environnementale en minimisant l'impact négatif sur l'environnement et la santé humaine. Le cours vise a étudié en détaille les dix principes de la chimie verte
Prévention
Économie d'atomes
Synthèse moins dangereuse
Conception de produits plus sûrs
Sécurité auxiliaire.
Énergie moins intensive
Utilisation des ressources renouvelables
Réduction des déchets
Catalyse
Dégradation
- Enseignant: chemat zoubida
Intitulé du Master : Chimie Analytique
Intitulé de l’UE : UED2.1
Intitulé de la matière : Chimie Verte; en alternance Santé et Sécurité Alimentaire
Crédits : 2
Coefficients : 1
- Enseignant: Daghbouche Yasmina